
Rektumkarzinom (Mastdarmkrebs)
Mastdarmkrebs
Bösartige Dickdarmtumoren, die im Enddarm lokalisiert sind bezeichnet man als Mastdarmkrebs oder Rektumkarzinom. Das Rektumkarzinom ist häufig und macht mindestens ein Drittel aller im Dickdarm lokalisierten Tumoren aus, die wiederum an zweiter Stelle in der Häufigkeitsstatistik bösartiger Erkrankungen in Deutschland stehen. Der Enddarm ist ein spezialisierter Teil des Dickdarms, der vor allen Dingen die Aufgabe eines Kontinenzorgans übernimmt, das heißt, dass der Enddarm neben dem Afterschließmuskel das wesentliche Organ für das Stuhlhalten und die kontrollierte Entleerung des Darms darstellt.
Wir teilen den Enddarm in drei Bereiche eine. Dabei ist die Behandlung von Tumoren des oberen Drittels der Behandlung der Tumoren der höher gelegenen Dickdarmabschnitte ähnlich, während die Behandlung von Tumor des mittleren und unteren Drittels sich in den meisten Fällen deutlich hiervon unterscheidet.
Im nachfolgenden Kapitel wird zunächst nur auf die Behandlung der sporadischen Tumoren eingegangen, wobei die Grundsätze auch für viele der genannten Sonderformen angewendet werden.
Die Behandlung des Rektumkarzinoms ist technisch anspruchsvoll. Der Enddarm ist im Becken unmittelbar von anderen Organen, Nerven und Blutgefäßen umgeben, die bei einer Operation unbedingt geschont werden müssen, um alle wichtigen Funktionen, wie die Blasenfunktion, die Sexualfunktion und natürlich die Stuhlhaltefunktion (Kontinenz) aufrecht zu erhalten. Trotz der Nähe zum Afterschließmuskel kann in unserer Klinik in rund 80- 90% der Patienten eine kontinenzerhaltende (schließmuskel-erhaltende) Operation angeboten werden. Eine Entfernung des Enddarms mit dem Afterschließmuskel und die Anlage eines dauerhaften künstlichen Darmausganges ist eigentlich nur noch bei unmittelbarem Befall des Schließmuskels durch den Tumor notwendig oder wird in seltenen Fällen durchgeführt, wenn der Schließmuskel funktionslos oder erheblich funktionsgestört ist und eine schließmuskelerhaltende Operation zu einer schweren Stuhlinkontinenz führen würde.
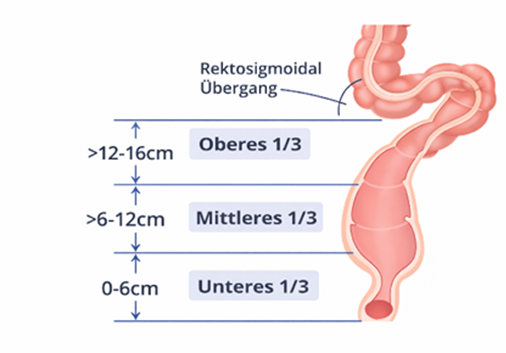
Abbildung 1: Einteilung des Rektumkarzinoms in drei Höhenbereiche
Gleichwohl treten nach schließmuskelerhaltenden Operationen bei jedem zweiten Patienten Störungen der Darmfunktion auf, die Symptome wie Inkontinenz, Veränderungen der Stuhlfrequenz, das Auftreten von dringlichem Stuhldrang und Schwierigkeiten, den Darm zu entleeren beinhalten und als anteriores Resektionssyndrom (Low Anterior Resection Syndrom oder kurz LARS) zusammenfasst werden. Ein LARS kann erheblich die Lebensqualität beeinflussen, so dass eine funktionelle Nachbetreuung oft notwendig ist (1, 2).
In den letzten zwei Jahrzehnten hat sich das Wissen um die Behandlung des Rektumkarzinoms erheblich vermehrt und eine Vielzahl neuer Behandlungstechniken hat dazu geführt, dass die Heilungschancen sich erheblich verbessert haben und mittlerweile vielleicht sogar besser ist, als bei Tumoren im höher gelegenen Dickdarm.
Auch wenn frühe Enddarmtumoren oft durch eine alleinige Operation geheilt werden können, sind an der Behandlung aller etwas weiter fortgeschrittenen Rektumkarzinome verschiedene Fachdisziplinen beteiligt. Neben der Chirurgie sind dies vor allem die auf die medikamentöse Tumortherapie spezialisierte Onkologen sowie die Strahlentherapeuten. Eine Reihe von Studien hat Hinweise darauf erbracht, dass bei Tumoren, die die Darmwand überschreiten oder die bereits Lymphknotenabsiedlungen gemacht haben, eine Kombination aus Strahlentherapie, Chemotherapie und Operation die beste Heilungschance bietet. Dabei hat sich gezeigt, dass bei einer solchen Kombinationsbehandlung die Anwendung einer Strahlen- und Chemotherapie vor einer Operation effektiver und zugleich besser verträglich ist, als die Anwendung nach der Operation. Da Strahlen- und Chemotherapie aber auch gewisse Nebenwirkungen haben und auch die Funktion der Beckenorgane nachteilig beeinflussen kann, wird durch eine eingehende Untersuchung des Tumors durch Ultraschall, Computertomographie und Kernspintomographie vor Beginn der Behandlung versucht, das Tumorstadium exakt festzulegen, um nur solche Tumoren mit einer Kombinationsbehandlung anzugehen, bei denen auch wirklich eine entsprechende Notwendigkeit besteht. Wir bezeichnen dies als „Staging“. Nach dem Staging wird das individuelle Behandlungskonzept für jeden Patienten im interdisziplinären Tumorboard festgelegt.
Der Erhalt der Stuhlkontinenz setzt in der Regel voraus, dass der Afterschließmuskel selber nicht tumorinfiltriert. Nur bei minimalem Tumorbefall im oberen Anteil des Afterschließmuskels kann in besonderen Situationen auch hier der Versuch einer kontinenzerhaltenden Operation vorgenommen werden.
Eine tumorgerechte Operation eines Enddarmtumors (Rektumkarzinoms) setzt in der Mehrzahl der Fälle eine komplette Entfernung des Enddarms (nicht des Schließmuskels) mit samt seinen Blut- und Lymphgefäßen voraus
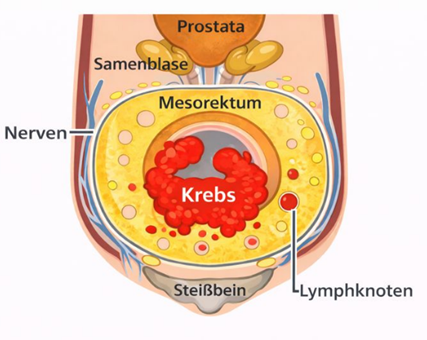
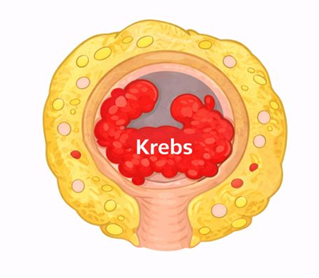
Abbildung 2: Grundprinzip der totalen mesorektalen Exzision
Wir bezeichnen dies Operation als „totale mesorektale Exzision“ oder abgekürzt als TME. Da zumindest ein 1 cm breites tumorfreies Darmsegment unterhalb des Tumors mit entfernt werden muss und viele Tumoren bereits sehr schließmuskelnahe lokalisiert sind, kann es sein, dass zum Erhalt der Darmfunktion zumindest Teile des Afterschließmuskels mit entfernt werden müssen. Wir sprechen von einer intersphinkteren Resektion. Die Durchführung solcher Eingriffe setzt Erfahrung mit besonderen operativen Techniken voraus, insbesondere die Herstellung einer Nahtverbindung direkt zwischen Darm und Schließmuskel „von untern“, also durch den Schließmuskel. Wir sprechen von einer „peranalen Anastomose“ mit der wir uns seit vielen Jahren beschäftigen (3-6). Bei sehr tiefen, großen Tumoren kann die Chance auf einen Schließmuskelerhalt vermutlich durch eine Kombination aus einer Präparation von bauchseitig und durch den Schließmuskel bessert werden. Wir sprechen von transanaler TME (TaTME, s.u.) (7-10). Zusammen mit der roboter-assistierten TME hat sich heute die Chance auf einen schließmuskelerhaltenden Eingriff deutlich verbessert und liegt in unseren Händen bei deutlich über 80%.
Eine schließmuskelerhaltende Totalentfernung des Enddarms (TME) führt häufig zu erheblichen Änderungen der Stuhlgewohnheiten. Insbesondere beklagen viele Patienten über eine erhöhte Stuhlfrequenz, Inkontinenzsymptome und dringlichen Stuhldrang. Letzteres bedeutet, dass bei Einsetzen des Gefühls den Darm entleeren zu müssen dem Betroffenen nur wenig Zeit bleibt, eine Toilette zu erreichen. Ursache ist die Entfernung des spezialisierten Enddarms und Ersatz durch ein nicht auf das Stuhlhalten spezialisierten Darmsegmentes meist durch eine direkte End-zu End-Nahtverbindung. Wir haben uns in den letzten 20 Jahren intensiv mit den Möglichkeiten zur Verbesserung diese Funktion durch verschieden Konstruktionen eines Ersatzenddarms beschäftigt (5, 11, 12). Dabei hat sich der Colon-J-Pouch als gute Methode gezeigt. Hierbei wird ein kleines Reservoir gebildet, welches die Stuhlfrequenz senkt und die Stuhlhaltefähigkeit verbessert. Auch eine Seit-zu End-Verbindung ist besser als die Rekonstruktion durch eine End-zu End-Verbindung. In seltenen Fällen können auch andere Rekonstruktionsformen sinnvoll sein, wie die ileocoecale Interposition. (13).
Bei frühen bösartigen Enddarmtumoren (Rektumkarzinomen) ist eine alleinige lokale Entfernung des Tumors möglich. Dies gilt für Tumoren kleiner 3 Zentimeter, die nicht die Muskelschicht der Darmwand erreicht haben und die mikroskopisch keine Zeichen besonderer Bösartigkeit aufweisen. Das Risiko bereits bestehender Lymphknotenabsiedlungen ist bei diesen Tumoren ausgesprochen gering. Am sichersten ist die Durchführung solcher Operationen unter videoendoskopische Sicht und damit mit Lupenvergrößerung. Wir bezeichnen diese Eingriffe als Transanale Minimalinvasive oder kurz TAMIS Operationen. Die Operationen sind zwar technisch aufwendig aber für den Betroffenen sehr wenig belasten.
Auch eine Totalentfernung des Enddarms mit den dazu gehörigen Blut- und Lymphgefäßen (= totale mesorektale Exzision kurz TME) kann von unten, durch den Schließmuskel erfolgen. Wir bezeichnen das Vorgehen als transanale TME (taTME). Auch wenn potentiell der gesamte Eingriff von unten durchführbar sein kann, wird er immer mit einer minimalinvasiven Operation von bauchseitig kombiniert, sodass der Eingriff früher auch als „Hybrid-TAMIS-TME“ geführt wird. Das Ziel des kombinierten Vorgehens von bauchseitig (transabdominal) und durch den Schließmuskel (transanal) liegt nicht in einer Verbesserung der Kosmetik sondern vielmehr in der sichereren Entfernung des Tumors und den besseren Möglichkeiten der Schonung der für den Erhalt der Blasen, Sexual- und Mastdarmfunktion notwendigen Nerven (7, 8, 14). Besonders bei großen und sehr schließmuskelnahen Tumoren kann die Methode helfen, einen Erhalt des Afterschließmuskels und damit der Kontinenz zu gewährleisten.
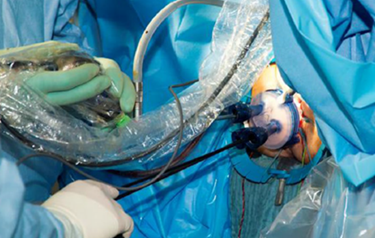
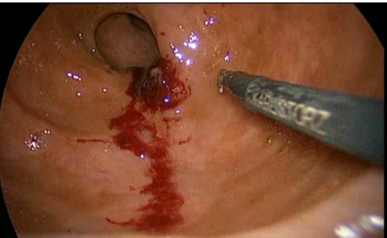
Abbildung 3a und 3b: Transanale minimalinvasive Präzisionschirurgie
Die Totalentfernung von Enddarm und Afterschließmuskel und Anlage eines bleibenden künstlichen Darmausganges ist nur selten notwendig, bieten aber bei großen Tumoren mit Beteiligung des Schließmuskels oder der Beckenbodenmuskulatur die einzige Chance auf Heilung. Diese ist zudem bei kompletter Entfernung des Tumors und Fehlen von Fernabsiedlungen gut. Um diese Tumoren wirklich sicher im Gesunden zu entfernen muss der Schließmuskel mit großen Teilen der Beckenbodenmuskulatur entfernt werden. Um den Defekt am Beckenboden zu decken, verwenden wir plastisch-chirurgische Lappenplastiken. So kann man einen Teil der Bauchdeckenmuskulatur durch entsprechende Präparation an den Beckenboden transponieren.
Das Leben mit einem dauerhaften künstlichen Darmausgang macht vielen Menschen verständlicher-weise Angst. Tatsächlich erreichen die meisten Betroffenen aber eine exzellente Lebensqualität. Viele Spülen den Darm einmal täglich und können hierdurch eine nahezu komplette Entleerung erreichen, so dass sie den Ausgang noch nicht einmal mit einem Beutel versorgen müssen. Wir sprechen von Irrigation. Auch sportliche Aktivitäten inklusive Schwimmen, können zu weiten Teilen ohne Einschränkungen vorgenommen werden. Sollte bei Ihnen die Anlage eines künstlichen Darmausganges notwendig sein, werden wir Sie frühzeitig durch unsere Stomatherapeutinnen beraten lassen.
Operationen von Enddarmtumoren werden in unserer Klinik nahezu ausschließlich in minimal-invasiver Technik („Knopflochtechnik“) durchgeführt. Aktuelle Studien belegenen nicht nur die Gleichwertigkeit der minimal-invasiven gegenüber der offen Chirurgie, sondern deuten bei fortgeschrittenen Tumorstadien sogar auf bessere Langzeitergebnisse nach minimal-invasiver Operation hin (15). Zudem ist die Erholung nach einem minimal-invasiven Eingriffe besser.
In der Regel werden Enddarmtumoren über vier Minischnitte von etwa einem Zentimeter durchgeführt. Die Bergung des tumortragenden Darmanteils erfolgt dann über einen Minischnitt in der „Bikini-Zone“.
Für die operative Behandlung von Enddarmtumoren nutzen wir bevorzugt den OP-Roboter (DaVinci-System). Der Roboter bietet die Möglichkeit, unter 10facher Vergrößerung und dreidimensionalem Bild sehr präzise, den tumortragenden Darmanteil zu entfernen und zugleich die für den Funktionserhalt wichtigen übrigen Beckenorgane, vor allem aber auch die Nervenstrukturen, die für
Blasen- Darm-, vor allem aber auch die Sexualfunktion von entscheidender Bedeutung sind maximal zu schonen. Eine aktuell publizierte Studie aus China konnte zeigen, dass durch den Einsatz des Roboters nicht bessere funktionelle, aber auch leicht besser onkologische Ergebnisse erreicht werden können (16).
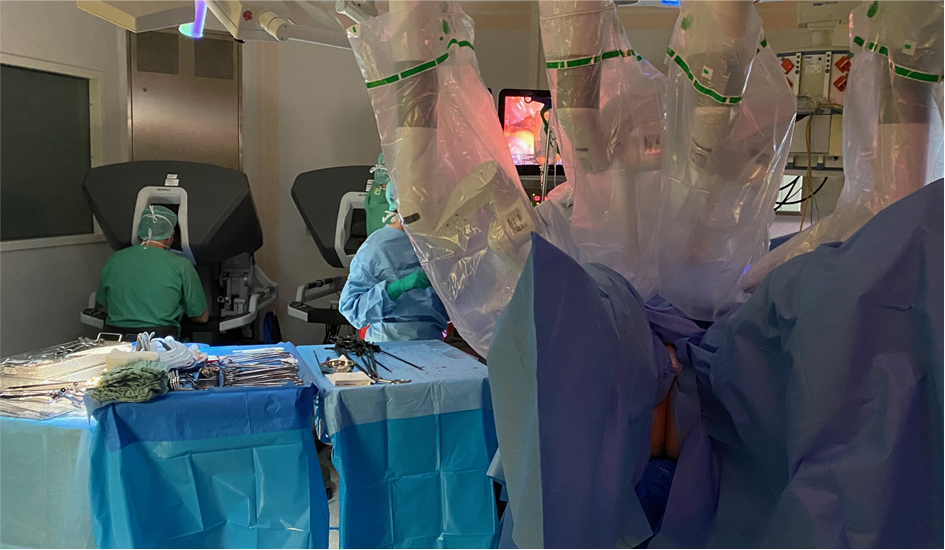
Abbildung 4: Präzisionschirurgie durch Anwendung eines DaVinci Operationsroboters
Abhängig von ihren biologischen Eigenschaften sprechen einige Geschwulste sehr gut auf eine medikamentöse Therapie an. Dies gilt besonders für viele erblich bedingte Darmkrebserkrankungen, die sogenannten hereditären Karzinome. Sie entstehen, weil im Körper eine Fehlfunktion der Reparatureiweiße vorliegen, die sonst Kopierfehler im Erbgut der Zelle korrigieren, die regelmäßig bei der Zellteilung auftreten. Diese Tumoren entstehen oft bei jungen Menschen und haben grundsätzlich die Eigenschaft einer hohen Immunogenität. Sie könnten vom körpereigene Abwehrsystem erkannt und zerstört werden, wenn die Tumorzelle nicht spezielle Substanzen produzieren würden, die als Schutzmechanismus gegen die immunologische Zerstörung der Tumorzelle wirken. Mittlerweile stehen uns Medikamente zur Verfügung, mit denen wir diesen Mechanismus ausschalten kann. Wir bezeichnen sie als Immuncheckpointinhibitoren. Bei diesen speziellen Tumoren (den sogenannte „mikrosatelliteninstabile Tumor“) führt eine alleinige Therapie mit einem Immuncheckpointinhibitor oft zu einem vollständigen und nachhaltigen Verschwinden des Tumors, wodurch in den meisten Fällen auf eine Operation verzichtet werden kann (17, 18). Selten können auch nicht erbliche, sogenannte sporadische Karzinome mikrosatelliteninstabil und damit für eine entsprechende Therapie zugängig sein. Lieder sind dies beim Rektumkarzinom nur 1-3 Prozent aller Tumoren.
Eine weitere Möglichkeit der nicht operativen Therapie besteht bei einem sehr guten Ansprechen auf eine Vorbehandlung des Tumors durch eine Radiochemotherapie. Bei einer ausreichend intensiven Vorbehandlung (i.d.R. Bestrahlung + Kombinationschemotherapie) können in Abhängigkeit von Tumorgröße und Lokalisation rund ein Drittel der Tumoren komplette verschwinden. Wir bezeichnen diese Art der Vorbehandlung als „Totale neoadjuvante Therapie (TNT)“. Ein Begriff der signalisiert, dass alle Behandlungsoptionen die früher entweder nach einer Operation oder teilweise vorher und hinterher verabreicht wurden, jetzt vollständig vor der Operation gegeben werden. Das komplette Verschwinden des Tumors wird als Vollremission bezeichnet.
In diesen Fällen kann auch auf eine Operation verzichtet werden, wenn eine sehr engmaschige Nachsorge mit Endoskopie und PET-CT für insgesamt 5 Jahre durchgeführt wird, die innerhalb der ersten zwei Jahre in 3–4-monatigen Abständen vorgenommen werden muss. Das Risiko eine erneuten Tumorwachsums liegt bei 25-30%. Nur unter einer so engmaschigen Nachsorge kann sichergestellt werden, dass durch eine dann durchgeführte Operation, die guten Chancen auf eine Heilung der Tumorerkrankung aufrechterhalten werden.
Auch unabhängig von dem möglichen Ziel, auf eine Operation ganz verzichten zu könne, hat der Einsatz von Chemo- und Strahlentherapie einen festen Stellenwert bei der Behandlung des Rektumkarzinoms. Grob gesagt werden Tumoren, die die Darmwand überschreiten und / oder in die lokalen Lymphknoten bereits Tumorabsiedlungen gesetzt haben, eher kombiniert durch Bestrahlung, Chemotherapie und Operation (multimodal) behandelt.
Wegen besserer Wirksamkeit wird die Bestrahlug, wenn sie notwendig ist, vorzugsweise präoperativ, also vor der Operation verabreicht und auch die Chemotherapie wir in zunehmendem Maße vor der Operation gegeben.
Dabei verfolgt die Vorbehandlung zwei Ziele: Erstens, soll das Risiko eines Lokalrezidives (Wiederauftreten von Tumor im Becken) minimieren werden, zweiten, das Auftreten von Fernmetastasen. Für die Einschätzung des Risikos von Metastasen ist vor allem das Tumorstadium entscheidend. So steigt das Risiko für eine Lokalrezidiv vor allem, bei darmwandüberschreitenden Tumoren im schließmuskelnahen Anteil des Enddarms und bei solchen Tumoren, die Absiedlungen in die lokalen Lymphknoten gemacht haben. Für das Lokalrezidivrisiko ist vor allem aber die Qualität der Operation entscheidend. Wenn Tumoren nicht mehr als 2 mm an den Rand des den Darm umgebenden Fettgewebes heranreichen, kann bei guter Operationstechnik das Lokalrezidivrisiko auch bei Verzicht auf Strahlen- und Chemotherapie auf etwas 2-3% reduziert werden.
Das Risiko für Fernabsiedlungen liegt bei den Tumoren etwas 10fach höher und ist wahrscheinlich nur wenig durch die Operationstechnik zu beeinflussen. Aus diesem Grunde besteht bei vielen fortgeschritteneren Tumor auch unabhängig von dem Ziel, ggf. auf eine Operation verzichten zu können, eine Indikation für eine (radio)chemotherapeutische Vorbehandlung.
Der zweite wichtige Punkt in der Therapieentscheidung ist die Tumorlokalisation. Sehr schließmuskelnahe lokalisierte Rektumkarzinom sind technisch deutlich schwieriger unter Schließmuskel erhalt zu operieren als höher gelegene Tumoren und haben dadurch tendenziell ein höheres Lokalrezidivrisiko. Zudem ist bei ganz schließmuskelnah lokalisierten Tumoren eine Teil- oder sogar eine Totalentfernung des Schließmuskels notwendig, was im erstgenannten Fall ein hohes Risiko für funktionelle Probleme, im letztgenannten Fall sogar die Anlage eines permanenten künstlichen Darmausganges notwendig macht.
So attraktiv eine nichtoperative Behandlung des Rektumkarzinoms auf den ersten Blick erscheint, müssen auch einige Probleme in der Therapieplanung berücksichtig und intensiv besprochen werden. Sieht man einmal von den vergleichsweise selten auftretenden mikrosatelliteninstabilen Tumoren ab, die durch eine alleinige Immuntherapie behandelt werden können (s.o.), bedarf eine Vorbehandlung des Enddarmtumors mit dem Ziel, sie nicht operieren zu müssen, einer Kombination aus einer Strahlentherapie und einer Kombinationschemotherapie. Diese haben nicht unerhebliche Risiken:
- Die Strahlentherapie als solche kann zu erheblichen funktionellen Problemen führen. So finden sich schwerwiegende Darmfunktionsstörungen im Sinne eines LARS-Syndroms auch bei 25-30% der Betroffen nach Radiochemotherapie auch ohne Operation. Auch Störungen der Sexualfunktion können als Folge der Bestrahlung auftreten.
- Auch die Chemotherapie hat Nebenwirkung. Eine der relevantesten ist das Auftreten sogenannter Polyneuropathien, also Missempfindungen vor allem in Zehen und Fingern, die vor allem die Feinmotorik erheblich beinträchtigen können.
- Auch die Chemotherapie hat Nebenwirkung. Eine der relevantesten ist das Auftreten sogenannter Polyneuropathien, also Missempfindungen vor allem in Zehen und Fingern, die vor allem die Feinmotorik erheblich beinträchtigen können.
- Die Behandlung dauert lange: alles in allem ist man rund 6 Monate unter Therapie.
- Das Ansprechen auf die Behandlung ist schlecht vorhersagbar. Grob geschätzt kann nur bei einem von drei Patienten nach einer Radiochemotherapie auf eine Operation verzichtet werden. Das bedeutet auch, dass bei zwei von drei Pateinten sich die unerwünschten Folgen aller Behandlungsmodalitäten (Operation, Strahlentherapie, Chemotherapie) aufsummieren oder sogar potenzieren.
- Zudem verbleibt ein Risiko von mindestens 25% für eine erneutes Tumorwachstum, was eine sehr engmaschige und oft auch als psychisch belastend empfundene Nachsorge notwendig macht.
Auch wenn das Behandlungskonzept immer individuell besprochen werden muss, können eine paar strategischen Überlegungen, die wir bei der Wahl des Therapieverfahrens zugrunde legen, hier festgehalten werden.
- Bei Tumoren, die relative weit vom Schließmuskel entfernt lokalisiert und nicht zu weit fortgeschritten sind, empfehlen wir eher eine primäre Operation oder bei etwas weiter fortgeschritteneren oder aggressiveren Tumoren eine Operation nach einer alleinigen Chemotherapie (ohne Bestrahlung). Eine Strahlentherapie wird empfohlen, wenn aufgrund der MRT-Untersuchung ein hohes Risiko besteht, den Tumor nicht im gesunden herausoperiert zu bekommen.
- Für schließmuskelnahe Tumoren, die nur durch eine Teil- oder Totalentfernung des Afterschließmuskels behandelt werden können, empfehlen wir in aller Regel eine intensive radiochemotherapeutische Vorbehandlung (TNT-Konzept) um die Chancen zu nutzen, bei gutem Ansprechen auf eine Operation ganz verzichten zu können. Schließmuskelnaht Tumoren haben wahrscheinlich eine etwas größere Chance, auf eine Radiochemotherapie vollständig zu verschwinden. Bei gutem, aber nicht ganz vollständigem Ansprechen führen wir gelegentlich auch nur eine lokale Entfernung des verbliebenen Tumorrestes durch ohne aber den gesamten Enddarm zu entfernen.
- Bei sehr frühen Tumoren ohne Hinweis auf Lymphknotenabsiedlungen kann gelegentlich eine alleinige lokale Tumorentfernung ausreichend sein (s.u.)
Durch die Totalentfernung des Enddarms und Ersatz durch ein anderes, für die besonderen Aufgaben des Enddarms nicht spezialisierten Darmsegmentes, kommt es nicht selten zu Störungen der Darmfunktion, die wir als anteriore Resektionssyndrom bezeichnen (s.o.). Das Syndrom kann bei starker Ausprägung erheblich die Lebensqualität beeinträchtigen, ist aber in der Mehrzahl der Fälle sehr effektiv zu behandeln (1, 2).
Ansprechpartner

Univ.-Prof. Dr. med.
Andreas Rink
Leiter Sektion Minimalinvasive Onkologische Chirurgie

Dr. med.
Jan Peter Neuhaus
Oberarzt
Kontakt
Sekretariat
Tel: 0201 723 1155
Fax: 0201 723 5805
Ambulanz
Tel: 0201 723 1130
Stationen
AC1– Intensivstation
Tel: 0201 723 1181
AC2 – Interdisziplinäre Transplantstation
Tel: 0201 723 1182
AC3/4
Tel: 0201 723 1183
Tel: 0201 723 1184
AC5
Tel: 0201 723 1185
Literatur
1. Rink AD. Treatment of low anterior resection syndrome (LARS). Coloproctology. 2023;45(1):16-26.
2. Müller AB, Rink A. D. . Kontinenz- und Stuhlentleerungsmanagement nach tiefer anteriorer Rektumresektion. Coloproctology. 2024 47:22-8.
3. Rink AD, Kneist W, Radinski I, Guinot-Barona A, Lang H, Vestweber KH. Differences in ano-neorectal physiology of ileoanal and coloanal reconstructions for restorative proctectomy. Colorectal Dis. 2010;12(4):342-50.
4. Rink AD, Radinski I, Vestweber KH. Does mesorectal preservation protect the ileoanal anastomosis after restorative proctocolectomy? J Gastrointest Surg. 2009;13(1):120-8.
5. Rink AD, Sgourakis G, Sotiropoulos GC, Lang H, Vestweber KH. The colon J-pouch as a cause of evacuation disorders after rectal resection: myth or fact? Langenbecks Arch Surg. 2009;394(1):79-91.
6. Rink AD, Nagelschmidt M, Radinski I, Vestweber KH. Evaluation of vector manometry for characterization of functional outcome after restorative proctocolectomy. Int J Colorectal Dis. 2008;23(8):807-15.
7. Rink AD, Kauff DW, Paschold M, Vestweber KH, Lang H, Kneist W. [Hybrid TAMIS total mesorectal excision : A new perspective in treatment of distal rectal cancer – Technique and results]. Der Chirurg; Zeitschrift fur alle Gebiete der operativen Medizen. 2015.
8. Kneist W, Rink AD, Kauff DW, Konerding MA, Lang H. Topography of the extrinsic internal anal sphincter nerve supply during laparoscopic-assisted TAMIS TME: five key zones of risk from the surgeons‘ view. Int J Colorectal Dis. 2015;30(1):71-8.
9. Rink AD, Aigner F, Biebl M, Furst A, Kneist W. [Transanal total mesorectal excision : A useful complementary method for minimally invasive surgery of rectal cancer]. Chirurg. 2019;90(6):487-9.
10. Zeng Z, Luo S, Zhang H, Wu M, Ma D, Wang Q, et al. Transanal vs Laparoscopic Total Mesorectal Excision and 3-Year Disease-Free Survival in Rectal Cancer: The TaLaR Randomized Clinical Trial. JAMA. 2025;333(9):774-83.
11. Rink AD, Haaf F, Knupper N, Vestweber KH. Prospective randomised trial comparing ileocaecal interposition and colon-J-pouch as rectal replacement after total mesorectal excision. International journal of colorectal disease. 2007;22(2):153-60.
12. Rink AD, Vestweber KH. [Vulnerability of ileocoecal interposition pouch and colonic J-pouch to postoperative adjuvant radiotherapy]. Zentralblatt fur Chirurgie. 2002;127(9):769-74.
13. Rink AD, Vestweber B, Vestweber KH. Modified ileocecal interposition. The final sphincter-saving solution after failed salvage surgery for anastomotic complications of low anterior resection. Dig Surg. 2008;25(5):359-63.
14. Rink AD, Aigner, F., Biebl, M., Fürst A., Kneist W. Transanale totale mesorektale Exzision – eine sinnvolle Operationstechnik zur individualisierten Behandlung von Patienten mit Rektumkarzinom. Coloproctology. 2019;41:272-9.
15. Bonjer HJ, Deijen CL, Haglind E, Grp CIS. A Randomized Trial of Laparoscopic versus Open Surgery for Rectal Cancer Reply. New Engl J Med. 2015;373(2):194-.
16. Feng Q, Yuan W, Li T, Tang B, Jia B, Zhou Y, et al. Robotic vs Laparoscopic Surgery for Middle and Low Rectal Cancer: The REAL Randomized Clinical Trial. JAMA. 2025;334(2):136-48.
17. Rink ADK-V, S. Heilung ohne Operation und Radiochemotherapie beim lokal fortgeschrittenen, Mismatch-Reparatur-defizienten Rektumkarzinom? Coloproctology. 2022;44:35-6.
18. Cercek A, Lumish M, Sinopoli J, Weiss J, Shia J, Lamendola-Essel M, et al. PD-1 Blockade in Mismatch Repair-Deficient, Locally Advanced Rectal Cancer. N Engl J Med. 2022;386(25):2363-76.